北京百泰派克生物科技有限公司品牌商
9 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0
- 0
- 2
- 2
推荐产品
技术资料/正文
蛋白质组学:原理、技术及应用
2805 人阅读发布时间:2023-06-28 14:32
什么是蛋白质组?
蛋白质是由氨基酸组成的生物分子。蛋白质是生命所必需的,具有结构、新陈代谢、运输、免疫、信号和调节等许多功能。
“蛋白质组”一词是澳大利亚博士生马克-威尔金斯于1994年在意大利锡耶纳举行的研讨会上首次提出的。这是一个笼统的术语,指的是有机体可以表达的所有蛋白质。每个物种都有自己独特的蛋白质组。
与基因组(每个生物体内的完整基因集)不同,蛋白质组的组成随着时间的推移和整个生物体的变化而不断变化。因此,当科学家提到蛋白质组时,他们有时也指的是给定时间点的蛋白质组(例如胚胎与成熟生物体),或者生物体内特定细胞类型或组织的蛋白质组。
什么是蛋白质组学?
蛋白质组学是对蛋白质组的研究—研究不同的蛋白质如何相互作用以及它们在生物体内扮演的角色。
虽然蛋白质表达可以通过研究mRNA的表达来推断,因为mRNA是连接基因和蛋白质之间的桥梁,但mRNA表达水平并不总能准确反映蛋白质的表达水平。此外,mRNA的研究不考虑蛋白质翻译后修饰、切割、复合物形成和定位、或可以产生的许多变异mRNA转录本;所有这些都是决定蛋白质功能的关键。
第一批符合“蛋白质组”研究标签的实验是在1975年随着二维蛋白质电泳法的发展而进行的。
然而,20多年后,随着质谱(MS)技术的发展,每个样品中多种蛋白质的真正高通量鉴定才成为可能。
从那时起,MS的灵敏度和准确性已经提高到可以可靠地检测低至全摩尔范围的蛋白质(每 1018个分子1个目标蛋白质分子),并且开发和优化了各种其他蛋白质组学技术。

1、Timp W, Timp G. Beyond mass spectrometry, the next step in proteomics. Sci Adv. 2020;6(2):eaax8978.
2、Wilkins M. Proteomics data mining. Expert Rev Proteomics. 2009;6(6):599-603.
3、Beynon RJ. The dynamics of the proteome: strategies for measuring protein turnover on a proteome-wide scale. Brief Funct Genomic Proteomic. 2005;3(4):382-390.
4、Garrels JI. Proteome. In: Brenner S, Miller JH, eds. Encyclopaedia of Genetics. London: Academic Press; 2001:1575-1578.
5、Graves PR, Haystead TA. Molecular biologist's guide to proteomics. Microbiol Mol Biol Rev. 2002;66(1):39-63. doi:10.1128/mmbr.66.1.39-63.2002.
6、Andersen JS, Mann M. Functional genomics by mass spectrometry. FEBS Lett. 2000;480(1):25-31.
7、Bekker-Jensen DB, Martínez-Val A, Steigerwald S, et al. A compact quadrupole-orbitrap mass spectrometer with FAIMS interface improves proteome coverage in short LC gradients. Mol Cell Proteomics. 2020;19(4):716-729.
8、Aslam B, Basit M, Nisar MA, Khurshid M, Rasool MH. Proteomics: Technologies and their applications. J Chromatogr Sci. 2017;55(2):182-196.
9、 Chandramouli K, Qian PY. Proteomics: challenges, techniques and possibilities to overcome biological sample complexity. Hum Genomics Proteomics. 2009;2009:239204.
10、Zhang Y, Fonslow BR, Shan B, Baek MC, Yates JR 3rd. Protein analysis by shotgun/bottom-up proteomics. Chem Rev. 2013;113(4):2343-2394.
11、Zhang H, Ge Y. Comprehensive analysis of protein modifications by top-down mass spectrometry. Circ Cardiovasc Genet. 2011;4(6):711.
12、Perez‐Riverol Y, Moreno P. Scalable data analysis in proteomics and metabolomics using BioContainers and workflows engines. Proteomics. 2020;20:1900147.
13、Hu A, Noble WS, Wolf-Yadlin A. Technical advances in proteomics: new developments in data-independent acquisition. F1000Res. 2016;5:F1000 Faculty Rev-419.
14、Ison J, Rapacki K, Ménager H, et al. Tools and data services registry: a community effort to document bioinformatics resources. Nucleic Acids Res. 2016;44(D1):D38-D47.
15、Henry VJ, Bandrowski AE, Pepin AS, Gonzalez BJ, Desfeux A. OMICtools: an informative directory for multi-omic data analysis. Database. 2014;2014:bau069.
16、Afgan E, Baker D, Batut B, et al. The Galaxy platform for accessible, reproducible and collaborative biomedical analyses: 2018 update. Nucleic Acids Res. 2018;46(W1):W537-W544.
17、Tsiamis V, Ienasescu H, Gabrielaitis D, Palmblad M, Schwämmle V, Ison J. One thousand and one software for proteomics: Tales of the toolmakers of science. J Proteome Res. 2019;18(10):3580-3585.
18、Cole BS, Moore JH. Eleven quick tips for architecting biomedical informatics workflows with cloud computing. PLoS Comput Biol. 2018;14(3):e1005994.
19、Lawlor B, Sleator RD. The democratization of bioinformatics: A software engineering perspective. GigaScience. 2020;9(6):giaa063.
百泰派克生物科技七大检测平台

蛋白质是由氨基酸组成的生物分子。蛋白质是生命所必需的,具有结构、新陈代谢、运输、免疫、信号和调节等许多功能。
“蛋白质组”一词是澳大利亚博士生马克-威尔金斯于1994年在意大利锡耶纳举行的研讨会上首次提出的。这是一个笼统的术语,指的是有机体可以表达的所有蛋白质。每个物种都有自己独特的蛋白质组。
与基因组(每个生物体内的完整基因集)不同,蛋白质组的组成随着时间的推移和整个生物体的变化而不断变化。因此,当科学家提到蛋白质组时,他们有时也指的是给定时间点的蛋白质组(例如胚胎与成熟生物体),或者生物体内特定细胞类型或组织的蛋白质组。
什么是蛋白质组学?
蛋白质组学是对蛋白质组的研究—研究不同的蛋白质如何相互作用以及它们在生物体内扮演的角色。
虽然蛋白质表达可以通过研究mRNA的表达来推断,因为mRNA是连接基因和蛋白质之间的桥梁,但mRNA表达水平并不总能准确反映蛋白质的表达水平。此外,mRNA的研究不考虑蛋白质翻译后修饰、切割、复合物形成和定位、或可以产生的许多变异mRNA转录本;所有这些都是决定蛋白质功能的关键。
第一批符合“蛋白质组”研究标签的实验是在1975年随着二维蛋白质电泳法的发展而进行的。
然而,20多年后,随着质谱(MS)技术的发展,每个样品中多种蛋白质的真正高通量鉴定才成为可能。
从那时起,MS的灵敏度和准确性已经提高到可以可靠地检测低至全摩尔范围的蛋白质(每 1018个分子1个目标蛋白质分子),并且开发和优化了各种其他蛋白质组学技术。
蛋白质组学可以回答哪些关键问题?
广义而言,蛋白质组学研究为蛋白质水平上的健康和疾病过程提供了全局视角。为此,每个蛋白质组学研究通常集中在目标生物的蛋白质组的一个或多个方面,以慢慢建立现有的知识:
广义而言,蛋白质组学研究为蛋白质水平上的健康和疾病过程提供了全局视角。为此,每个蛋白质组学研究通常集中在目标生物的蛋白质组的一个或多个方面,以慢慢建立现有的知识:

蛋白质组学:技术
低通量方法:
1.基于抗体的方法
ELISA(酶联免疫吸附测定)和蛋白质印迹等技术依赖于靶向特定蛋白质或表位的抗体的可用性来鉴定蛋白质并量化其表达水平。
2.基于凝胶的方法
二维凝胶电泳(2DE或2D-PAGE)是第一个开发的蛋白质组学技术,它利用电流根据电荷(第一维)和质量(第二维)分离凝胶中的蛋白质。差异凝胶电泳(DIGE)是二维电泳的一种改良形式,它使用不同的荧光染料,可以在同一凝胶上同时比较两至三个蛋白质样本。这些基于凝胶的方法用于在通过例如质谱法(MS)进行进一步分析之前分离蛋白质以及相对表达谱分析。
3.基于色谱的方法
基于色谱的方法可用于从复杂的混合物(如细胞裂解物)中分离和纯化蛋白质。例如,离子交换色谱基于电荷分离蛋白质,尺寸排阻色谱根据蛋白质的分子大小分离蛋白质,亲和色谱采用特异性亲和配体与其靶蛋白之间的可逆相互作用(例如,使用凝集素纯化IgM和IgA分子)分离纯化蛋白质。这些方法可用于纯化和鉴定感兴趣的蛋白质以及制备蛋白质样品以供下游MS等进一步分析。
高通量方法:
1.分析型、功能型和反相微阵列
蛋白质微阵列将少量样品涂在“芯片”上进行分析(有时以具有化学修饰表面的载玻片的形式出现)。特异性抗体可以固定在芯片表面,并用于捕获复杂样品中的靶蛋白。这被称为分析型蛋白微阵列,这种类型的微阵列用于测量样品中蛋白质的表达水平和结合亲和力。功能型蛋白质微阵列用于表征蛋白质功能,例如蛋白质-RNA相互作用和酶-底物周转。在反相蛋白质微阵列中,来自健康组织与病变组织或未处理与处理细胞的蛋白质与芯片结合,然后用针对目标蛋白质的抗体探测芯片。
2.基于质谱的蛋白质组学
蛋白质的分离有几种“无凝胶”方法,包括同位素编码亲和标记(ICAT)、细胞培养中氨基酸稳定同位素标记(SILAC)和相对和绝对定量等压标记(iTRAQ)。这些方法可以用于定量和比较/差异蛋白质组学。还有少数其他定量的技术,如多维蛋白质鉴定技术(MudPIT),其优点是快速和便捷。其他用于蛋白质分离的无凝胶色谱技术包括气相色谱(GC)和液相色谱(LC)。
质谱工作流程
无论蛋白质样品如何分离,下游MS工作流程都包括三个主要步骤:
3.检测离子。
当样品用非凝胶技术(如iTRAQ或SILAC)分离,进行下游质谱分析时,样品可直接输入质谱仪。而使用基于凝胶的技术时,首先需要从凝胶中切出蛋白质条带并进行消化,然后通过LC分离或直接进行MS分析。
低通量方法:
1.基于抗体的方法
ELISA(酶联免疫吸附测定)和蛋白质印迹等技术依赖于靶向特定蛋白质或表位的抗体的可用性来鉴定蛋白质并量化其表达水平。
2.基于凝胶的方法
二维凝胶电泳(2DE或2D-PAGE)是第一个开发的蛋白质组学技术,它利用电流根据电荷(第一维)和质量(第二维)分离凝胶中的蛋白质。差异凝胶电泳(DIGE)是二维电泳的一种改良形式,它使用不同的荧光染料,可以在同一凝胶上同时比较两至三个蛋白质样本。这些基于凝胶的方法用于在通过例如质谱法(MS)进行进一步分析之前分离蛋白质以及相对表达谱分析。
3.基于色谱的方法
基于色谱的方法可用于从复杂的混合物(如细胞裂解物)中分离和纯化蛋白质。例如,离子交换色谱基于电荷分离蛋白质,尺寸排阻色谱根据蛋白质的分子大小分离蛋白质,亲和色谱采用特异性亲和配体与其靶蛋白之间的可逆相互作用(例如,使用凝集素纯化IgM和IgA分子)分离纯化蛋白质。这些方法可用于纯化和鉴定感兴趣的蛋白质以及制备蛋白质样品以供下游MS等进一步分析。
高通量方法:
1.分析型、功能型和反相微阵列
蛋白质微阵列将少量样品涂在“芯片”上进行分析(有时以具有化学修饰表面的载玻片的形式出现)。特异性抗体可以固定在芯片表面,并用于捕获复杂样品中的靶蛋白。这被称为分析型蛋白微阵列,这种类型的微阵列用于测量样品中蛋白质的表达水平和结合亲和力。功能型蛋白质微阵列用于表征蛋白质功能,例如蛋白质-RNA相互作用和酶-底物周转。在反相蛋白质微阵列中,来自健康组织与病变组织或未处理与处理细胞的蛋白质与芯片结合,然后用针对目标蛋白质的抗体探测芯片。
2.基于质谱的蛋白质组学
蛋白质的分离有几种“无凝胶”方法,包括同位素编码亲和标记(ICAT)、细胞培养中氨基酸稳定同位素标记(SILAC)和相对和绝对定量等压标记(iTRAQ)。这些方法可以用于定量和比较/差异蛋白质组学。还有少数其他定量的技术,如多维蛋白质鉴定技术(MudPIT),其优点是快速和便捷。其他用于蛋白质分离的无凝胶色谱技术包括气相色谱(GC)和液相色谱(LC)。
质谱工作流程
无论蛋白质样品如何分离,下游MS工作流程都包括三个主要步骤:
- 蛋白质/肽被质谱仪的离子源电离;
3.检测离子。
当样品用非凝胶技术(如iTRAQ或SILAC)分离,进行下游质谱分析时,样品可直接输入质谱仪。而使用基于凝胶的技术时,首先需要从凝胶中切出蛋白质条带并进行消化,然后通过LC分离或直接进行MS分析。
质谱电离源主要有两种,即:
其他不太常见的电离源包括化学电离、电子碰撞和辉光放电电离。
有四种主要的质量分析仪:
什么是串联质谱?
肽段可以进行多轮碎裂和质量分析,这一过程称为串联质谱、MS/MS或MSn。通过组合相同或不同的质量分析器,例如四极杆-TOF(Q-TOF)或三重四极杆(QQQ)MS,可以利用不同质量分析器的优势进一步提高蛋白质组分析的能力。简单的MS设置(如MALDI-TOF)仅用于肽质量数测量,而串联质谱仪可用于确定肽序列。
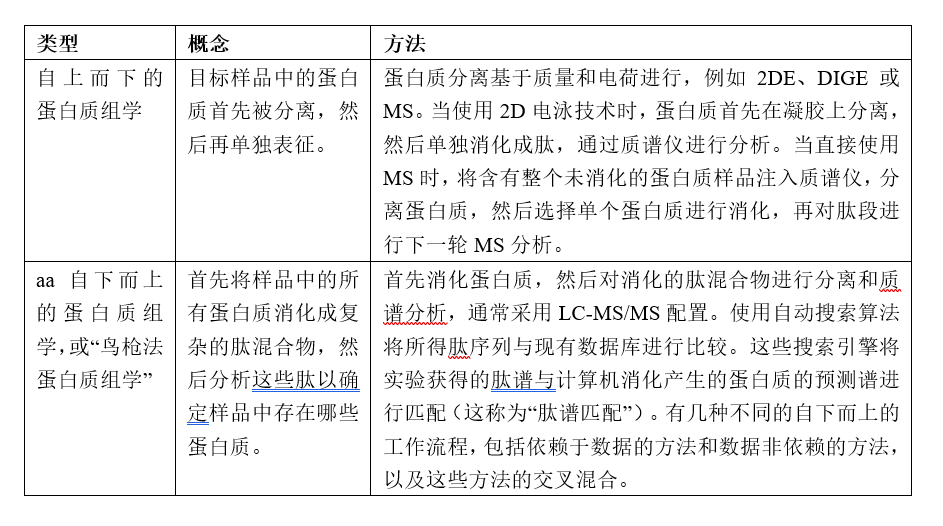
自上而下的蛋白质组学与自下而上的蛋白质组学
在自上而下的蛋白质组学中,首先分离目标样品中的蛋白质,然后再进行单独表征。
而自下而上的蛋白质组学(也称为“鸟枪”蛋白质组学),样品中的所有蛋白质首先被消化成复杂的肽混合物,然后通过分析这些肽以确定样品中存在哪些蛋白质。
- 基质辅助激光解吸电离(MALDI)
- 电喷雾电离(ESI)
其他不太常见的电离源包括化学电离、电子碰撞和辉光放电电离。
有四种主要的质量分析仪:
- 飞行时间(TOF)
- 离子阱
- 四极杆傅里叶变换离子回旋加速器(FTIC)
- 静电扇形和磁扇形是另外两种不太常用的质量分析器
什么是串联质谱?
肽段可以进行多轮碎裂和质量分析,这一过程称为串联质谱、MS/MS或MSn。通过组合相同或不同的质量分析器,例如四极杆-TOF(Q-TOF)或三重四极杆(QQQ)MS,可以利用不同质量分析器的优势进一步提高蛋白质组分析的能力。简单的MS设置(如MALDI-TOF)仅用于肽质量数测量,而串联质谱仪可用于确定肽序列。
自上而下的蛋白质组学与自下而上的蛋白质组学
在自上而下的蛋白质组学中,首先分离目标样品中的蛋白质,然后再进行单独表征。
而自下而上的蛋白质组学(也称为“鸟枪”蛋白质组学),样品中的所有蛋白质首先被消化成复杂的肽混合物,然后通过分析这些肽以确定样品中存在哪些蛋白质。

自上而下和自下而上的方法都有其各自的优缺点和各自更适合的应用。例如,自上而下的MS更适合研究不同的PTM和蛋白质亚型。然而,它受到分离复杂蛋白质混合物的挑战以及对较大蛋白质(特别是大于50-70 kDa)灵敏度降低的限制。
相比之下,虽然自下而上质谱中使用的肽(长度约为5-20个氨基酸)更容易分离、离子化和碎片化,但这种方法是对样品中最初存在的蛋白质的间接测量,并且严重依赖推断。目前已经开发出一种混合的“中下”方法,它使用比传统的自下而上的蛋白质组学更大的肽片段,从而可能允许更多独特的肽匹配。
蛋白质组学中的数据分析
蛋白质组学研究,特别是那些采用高通量技术的研究,会产生大量的数据。除了产生的大量数据外,蛋白质组学数据分析对于某些技术(如鸟枪法MS)也可能相对复杂。使这种复杂性增加的是可用于蛋白质组分析的一系列生物信息学工具。
蛋白质组学研究人员在尝试优化他们存储和分析蛋白质组学数据的方式时面临着许多挑战。
在设计蛋白质组学实验时,研究人员不仅需要考虑试剂和实验室设备的成本,还需要考虑数据存储和分析的成本,并且他们必须评估所需的生物信息学技能和计算资源水平。
蛋白质组学研究通常需要多个数据处理和分析步骤,这些步骤需要按特定顺序执行。为了满足这一需求,研究人员越来越习惯将所需的脚本、工具和软件组装成适合他们特定研究问题的定制蛋白质组分析方法。
蛋白质组学的应用
蛋白质组学的应用非常广泛和多样。下表仅列出了其中一些应用,并提供了使用这些方法的研究示例。
相比之下,虽然自下而上质谱中使用的肽(长度约为5-20个氨基酸)更容易分离、离子化和碎片化,但这种方法是对样品中最初存在的蛋白质的间接测量,并且严重依赖推断。目前已经开发出一种混合的“中下”方法,它使用比传统的自下而上的蛋白质组学更大的肽片段,从而可能允许更多独特的肽匹配。
蛋白质组学中的数据分析
蛋白质组学研究,特别是那些采用高通量技术的研究,会产生大量的数据。除了产生的大量数据外,蛋白质组学数据分析对于某些技术(如鸟枪法MS)也可能相对复杂。使这种复杂性增加的是可用于蛋白质组分析的一系列生物信息学工具。
蛋白质组学研究人员在尝试优化他们存储和分析蛋白质组学数据的方式时面临着许多挑战。
在设计蛋白质组学实验时,研究人员不仅需要考虑试剂和实验室设备的成本,还需要考虑数据存储和分析的成本,并且他们必须评估所需的生物信息学技能和计算资源水平。
蛋白质组学研究通常需要多个数据处理和分析步骤,这些步骤需要按特定顺序执行。为了满足这一需求,研究人员越来越习惯将所需的脚本、工具和软件组装成适合他们特定研究问题的定制蛋白质组分析方法。
蛋白质组学的应用
蛋白质组学的应用非常广泛和多样。下表仅列出了其中一些应用,并提供了使用这些方法的研究示例。

蛋白质组学的展望
目前,蛋白质组学研究严重依赖质谱。尽管这项技术已被证明很强大,但研究人员现在还在展望“超越MS”的蛋白质组学技术。虽然MS具有全摩尔灵敏度,但样品中仍需要存在数百万个目标分子才能被检测。这意味着低浓度靶分子在复杂的环境中可能无法检测到,例如人血清,除非首先富集。
科学家们仍在寻找高通量蛋白质组技术的圣杯,1)在目标蛋白质组的动态范围内具有极好的敏感性(例如,对于人类蛋白质组为107),2)可以直接读取整个蛋白质序列并识别它们的PTM,因此,3)不需要从理论蛋白质匹配的数据库中进行推断。
有几种候选的技术,尽管目前受到灵敏度、产量或成本的限制,但仍有可能主导蛋白质组学领域。其中包括新兴的荧光指纹法和尚未开发的用于蛋白质高通量单分子测序的亚纳米孔阵列。
随着蛋白质组学技术的预期进步,蛋白质组学数据分析的方法预计将迅速发展。例如,目前正大力推动云计算、软件容器和工作流系统等数据技术的发展,这些技术将使人们能够“民主化”地获得用于蛋白质组数据分析的顶级计算资源,而不论研究人员的位置、IT基础设施或计算专长如何。
参考文献目前,蛋白质组学研究严重依赖质谱。尽管这项技术已被证明很强大,但研究人员现在还在展望“超越MS”的蛋白质组学技术。虽然MS具有全摩尔灵敏度,但样品中仍需要存在数百万个目标分子才能被检测。这意味着低浓度靶分子在复杂的环境中可能无法检测到,例如人血清,除非首先富集。
科学家们仍在寻找高通量蛋白质组技术的圣杯,1)在目标蛋白质组的动态范围内具有极好的敏感性(例如,对于人类蛋白质组为107),2)可以直接读取整个蛋白质序列并识别它们的PTM,因此,3)不需要从理论蛋白质匹配的数据库中进行推断。
有几种候选的技术,尽管目前受到灵敏度、产量或成本的限制,但仍有可能主导蛋白质组学领域。其中包括新兴的荧光指纹法和尚未开发的用于蛋白质高通量单分子测序的亚纳米孔阵列。
随着蛋白质组学技术的预期进步,蛋白质组学数据分析的方法预计将迅速发展。例如,目前正大力推动云计算、软件容器和工作流系统等数据技术的发展,这些技术将使人们能够“民主化”地获得用于蛋白质组数据分析的顶级计算资源,而不论研究人员的位置、IT基础设施或计算专长如何。
1、Timp W, Timp G. Beyond mass spectrometry, the next step in proteomics. Sci Adv. 2020;6(2):eaax8978.
2、Wilkins M. Proteomics data mining. Expert Rev Proteomics. 2009;6(6):599-603.
3、Beynon RJ. The dynamics of the proteome: strategies for measuring protein turnover on a proteome-wide scale. Brief Funct Genomic Proteomic. 2005;3(4):382-390.
4、Garrels JI. Proteome. In: Brenner S, Miller JH, eds. Encyclopaedia of Genetics. London: Academic Press; 2001:1575-1578.
5、Graves PR, Haystead TA. Molecular biologist's guide to proteomics. Microbiol Mol Biol Rev. 2002;66(1):39-63. doi:10.1128/mmbr.66.1.39-63.2002.
6、Andersen JS, Mann M. Functional genomics by mass spectrometry. FEBS Lett. 2000;480(1):25-31.
7、Bekker-Jensen DB, Martínez-Val A, Steigerwald S, et al. A compact quadrupole-orbitrap mass spectrometer with FAIMS interface improves proteome coverage in short LC gradients. Mol Cell Proteomics. 2020;19(4):716-729.
8、Aslam B, Basit M, Nisar MA, Khurshid M, Rasool MH. Proteomics: Technologies and their applications. J Chromatogr Sci. 2017;55(2):182-196.
9、 Chandramouli K, Qian PY. Proteomics: challenges, techniques and possibilities to overcome biological sample complexity. Hum Genomics Proteomics. 2009;2009:239204.
10、Zhang Y, Fonslow BR, Shan B, Baek MC, Yates JR 3rd. Protein analysis by shotgun/bottom-up proteomics. Chem Rev. 2013;113(4):2343-2394.
11、Zhang H, Ge Y. Comprehensive analysis of protein modifications by top-down mass spectrometry. Circ Cardiovasc Genet. 2011;4(6):711.
12、Perez‐Riverol Y, Moreno P. Scalable data analysis in proteomics and metabolomics using BioContainers and workflows engines. Proteomics. 2020;20:1900147.
13、Hu A, Noble WS, Wolf-Yadlin A. Technical advances in proteomics: new developments in data-independent acquisition. F1000Res. 2016;5:F1000 Faculty Rev-419.
14、Ison J, Rapacki K, Ménager H, et al. Tools and data services registry: a community effort to document bioinformatics resources. Nucleic Acids Res. 2016;44(D1):D38-D47.
15、Henry VJ, Bandrowski AE, Pepin AS, Gonzalez BJ, Desfeux A. OMICtools: an informative directory for multi-omic data analysis. Database. 2014;2014:bau069.
16、Afgan E, Baker D, Batut B, et al. The Galaxy platform for accessible, reproducible and collaborative biomedical analyses: 2018 update. Nucleic Acids Res. 2018;46(W1):W537-W544.
17、Tsiamis V, Ienasescu H, Gabrielaitis D, Palmblad M, Schwämmle V, Ison J. One thousand and one software for proteomics: Tales of the toolmakers of science. J Proteome Res. 2019;18(10):3580-3585.
18、Cole BS, Moore JH. Eleven quick tips for architecting biomedical informatics workflows with cloud computing. PLoS Comput Biol. 2018;14(3):e1005994.
19、Lawlor B, Sleator RD. The democratization of bioinformatics: A software engineering perspective. GigaScience. 2020;9(6):giaa063.
百泰派克生物科技七大检测平台






